
Inhoud
Natriumacetaattrihydraat is een veel voorkomende en goedkope verbinding die wordt gebruikt voor verschillende toepassingen in voedingsmiddelen, industrieën en laboratoria. Het wordt gebruikt bij het beitsen, looien, als buffer en als hoofdbestanddeel van elektrische kompressen. Natriumacetaat wordt bestudeerd voor gebruik bij de denitrificatie van afvalwater als bestanddeel van nematiciden.
Voorbereiding
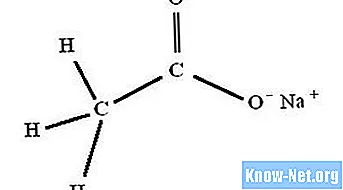
Natriumacetaattrihydraat, met de chemische formule NaC2H3O2.3H2O, wordt onmiddellijk gevormd door de reactie tussen azijnzuur (azijn) en natriumhydroxide, natriumcarbonaat of natriumbicarbonaat.
Naam en formule
De wetenschappelijke naam voor azijnzuur is ethanol. Om deze reden wordt natriumacetaat ook wel natriumetanoaat genoemd.
Organische chemici schrijven de structuur van natriumacetaat als NaC2H3O2.3H2O. In sommige situaties gebruiken ze echter de verkorte notatie "NaAc".
Voedselgebruik
In een een-op-een verhouding kunnen natriumacetaat en azijnzuur samen worden gekristalliseerd in een product dat natriumdiacetaat wordt genoemd. Dit product is zeer nuttig in de voedingsindustrie omdat het een bijna reukloze vaste stof is, maar "in situ" wordt het afgebroken tot zijn componenten. Zowel natriumacetaat als diacetaat hebben de GRAS-classificatie ontvangen (uit het Engels "algemeen erkend als veilig") door de Food and Drug Administration.
Natriumacetaat wordt in de vlees- en gevogelte-industrie gebruikt om de smaak te verbeteren. Diacetaat wordt voor een soortgelijk doel gebruikt en als remmer van de groei van ziekteverwekkers.
Medisch gebruik
Natriumacetaat in de geneeskunde wordt gebruikt om elektrolyten te herstellen. Het dient ook als diureticum.
De meest interessante toepassing ervan is in elektrische kompressen. Natriumacetaattrihydraat bevat drie moleculen kristallisatiewater. Verhit het tot 58 graden Celsius en dit water komt vrij uit het kristal. Ze lossen het gedehydrateerde natriumacetaat op en vervangen de vaste stof door een oplossing. Deze oplossing kan worden gekoeld zonder herkristallisatie om deze op kamertemperatuur te brengen. Indien gewenst kan deze vloeistof met de juiste prikkel gedwongen worden om weer te kristalliseren. Kristallisatie maakt warmte vrij, waardoor het gewenste lichaamsdeel wordt verwarmd.
Industrieel gebruik
Natriumacetaat is een alkalisch zout, dat het product is van de reactie van een sterke base met een zwak zuur. Daarom maken zijn basiciteit, evenals zijn lage kosten, het aantrekkelijk voor het neutraliseren van industriële minerale zuren uit lozingen.
Bij ongediertebestrijding wordt natriumacetaat bestudeerd voor gebruik als een bestanddeel van nematiciden. Nematoden kunnen als aas worden aangetrokken door natriumacetaat, net zoals insecten kunnen worden aangetrokken door feromonen.


